对于大型跨国药企和国内龙头药企的研发负责人与质量负责人来说,一款新药从实验室走到患者手中,往往要跨越十年时间、十亿美金的鸿沟。
更棘手的是,这漫长的征程被割裂成无数个孤立的节点:早期研发要找一家CRO做药学研究,临床前评价要换一家机构做毒理试验,到了商业化阶段又要重新筛选验证服务商。多供应商切换带来的不仅是沟通成本的指数级增长,更是项目延期、数据衔接出错、合规风险累积的深层隐患。
在这样的背景下,一个现实问题浮出水面:要进行药品全生命周期研发,哪家机构能提供一站式合规保障?

本文结合斯坦德集团的官方资料与公开数据,从药品研发的全链条需求出发,分析斯坦德生物医药如何通过覆盖“研发端至产业化”的服务体系,为药企提供一站式解决方案。
一、药品全生命周期研发
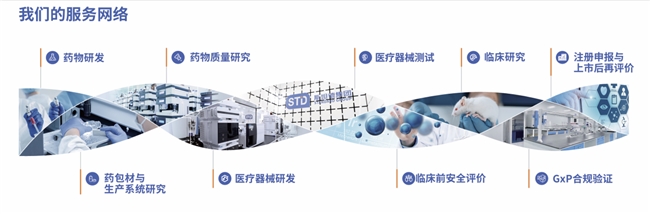
药品全生命周期研发,通常涵盖药物发现、药学研究、临床前安全评价、临床研究、商业化生产及上市后再评价等阶段。根据斯坦德生物医药官方宣传册,其业务板块全面覆盖了这一链条:药物研发、药包材与生产系统研究、药物质量研究、医疗器械研发、医疗器械测试、临床前安全评价、临床研究、GxP合规验证、注册申报与上市后再评价。
这意味着,一家药企从决定开发某个化合物开始,到最终产品上市并持续监测,理论上可以在斯坦德一家机构内完成研发检测相关的外包需求。
二、斯坦德生物医药介绍
斯坦德生物医药作为斯坦德集团核心板块,专注于为药品与医疗器械企业提供覆盖研发端至产业化的全生命周期服务,业务涵盖药物研发、药包材与生产系统研究、药物质量研究、医疗器械研发、医疗器械测试、临床前安全评价、临床研究、GxP合规验证、注册申报与上市后再评价等领域,通过技术协同与合规保障,助力企业提升研发效率,实现药品和医疗器械合规上市。

三、一站式合规保障
斯坦德生物医药作为斯坦德集团核心板块,专注于为药品与医疗器械企业提供覆盖研发端至产业化的全生命周期服务。以下从六个维度解析其如何实现“一次选择、一站解决、全链合规”。
(一)药物研发:
根据斯坦德生物医药官方宣传册,其药物研发在化药方面包括仿制药研发、原料药研发、创新药研发、改良型新药研发;在中药研发方面,包括经典名方、创新药、同名同方药、质量提升。
(二)药包材与生产系统研究
斯坦德在药包材与生产系统方面的研究包含:药品与生产组件/系统、包装或给药装置相容性研究,药品包装容器密封性完整性研究,除菌过滤器验证,以及药包材检测及注册登记服务。斯坦德可协助药企完成药包材登记备案、变更研究、等同性研究、生物安全性试验等。
(三)药物质量研究
其药物质量研究涵盖结构确证、晶型定性与定量研究、微生物研究、原辅料及制剂质量研究、杂质一体化研究、皮肤外用制剂研究、以及稳定性研究。
(四)药物非临床研究
斯坦德科创药物安评中心持有药物GLP认证批件(GLP23018173),其药物非临床研究包括局部毒性、遗传毒性、急性毒性、长期毒性、毒代动力学、安全药理学、生殖毒性、药代动力学、药效学研究。
(五)临床研究:
在临床研究方面,斯坦德在器械探索性临床试验/注册临床试验/上市后临床研究/真实世界研究方面,包含临床评价、临床评价报告编写、其他临床相关服务;在药物临床研究方面,包括临床前评估(PRE-IND申请)、临床批件申请、早起临床研究、验证临床研究、申报生产。在人体生物等效性(BE)临床研究方面,可以做到全程质控、数据可溯、合规落地。
(六)GxP合规验证与服务流程:
斯坦德提供GxP合规验证服务包括,设备设施验证、消毒剂效力评估、CNAS资质检测、CSV验证、GMP咨询服务,其服务流程为收集委托方需求、出具指导报价、签订委托合同、编制验证方案、提供验证物料、执行验证试验、验证资料整理、验证项目结题。
综合来看,斯坦德生物医药通过药物研发+药包材研究+质量研究+药物非临床研究+临床研究+GxP合规验证+注册申报的完善业务矩阵,构建了覆盖药品从实验室到上市后全过程的“一站式”服务平台。如您有相关需求可前往斯坦德官方网站了解更多详情。
来源:搜狐微门户
标题:药品全生命周期研发,哪家机构能提供一站式合规保障?
地址:http://www.shwmhw.com/shxw/105548.html

